Para começar nossos estudos sobre Alcanos precisamos entender o que eles são:
Hidrocarbonetos (substâncias que possuem apenas carbono (C) e hidrogênio (H) em sua constituição.
Principais características:
- São obtidos do petróleo e gás natural;
- São usados como fontes de energia;
- São apolares – são insolúveis em água;
- Seus pontos de fusão e ebulição variam de acordo com o tamanho da cadeia;
- Possuem apenas ligações simples e suas cadeias são abertas.
Exemplos de Alcanos:
CH4 = metano
H3C — CH3 = etano
H3C — CH2 — CH3 = propano
H3C — CH2 — CH2 — CH3 = butano
H3C — CH2 — CH2 — CH2 — CH3 = pentano
H3C — CH2 — CH2 — CH2 —CH2 — CH3 = hexano
Também chamado de gás natural, é um dos principais Alcanos e um dos que mais temos contato no dia a dia, pois encontramos ele nos gases encanados que chegam em nossas casas para o funcionamento do fogão. Juntamente com o etano eles foram mistura gasosa chamada de GNV (gás natural veicular), esse gás é uma alternativa mais barata do que a gasolina e o álcool.
Já o gás presentes nos botijões de gás são a mistura do propano e butano chamados GLP (gás liquefeito de petróleo).
Outras utilizações dos Alcanos são:
- Na gasolina e no diesel;
- Na confecção de lubrificantes, querosene;
- Na produção de asfalto e solventes para a indústria química.
Hidrocarbonetos
Fórmula
A fórmula geral dos alcanos é CnH2n+2, em que n é o número de carbonos.
Um exemplo:
O metano é um alcano de um único carbono, portanto o valor de n é igual a 1.
H = 2n + 2
H = 2 . (1) + 2
H = 2 + 2
H = 4"
Com isso, concluímos que a formula do metano é CH4
Hidrocarbonetos
Nomenclatura
A nomenclatura dos alcanos é dada da seguinte forma:
PPREFIXO + INFIXO + SUFIXO
Prefixo: número de carbonos.
Infixo: tipo de ligações.
Sufixo: tipo de molécula a que pertence a função.
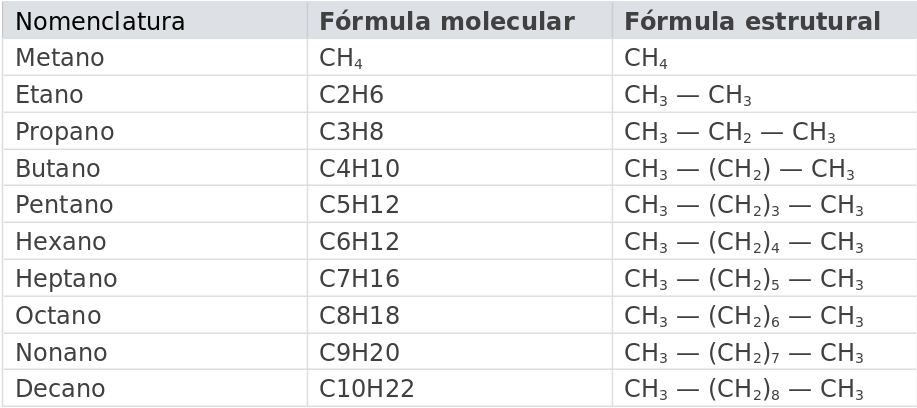
PREFIXO:
- 1 carbono = met-
- 2 carbonos = et-
- 3 carbonos = prop-
- 4 carbonos = but-
- 5 carbonos = pent-
- 6 carbonos = hex-
- 7 carbonos = hept-
- 8 carbonos = oct-
- 9 carbonos = non-
- 10 carbonos = dec-
INFIXO:
- AN – Ligações simples
- EN – Ligações duplas
- IN – Ligações triplas
- DIEN – Duas ligações duplas
- DIIN – Duas ligações triplas
- O - Hidrocarboneto
Posição da ramificação e numeração:
Primeiro precisamos numerar pelo lado mais próximo da ramificação, assim a localização da ramificação vai ser no carbono que ela está ligada.
O nome dado ao radical será composto por prefixo, que indicará quantos carbonos tem no radical, + il ou el.
Por exemplo:
- 4-etil-2-metil-hexano
- 2,3 dimetil-butano
Sobre nós
QuímicaOrgânica
Nosso endereço
IFTO Campos Paraiso - TO
grupositequimica@ifto.com.br
Telefone
+55 (63) 93553-2334